|
Коронавирусные инфекции кошек и собак вызываются представителями рода Coronavirus (семейство Coronaviridae). Основным проявлением коронавирусной инфекции у собак является диарея. V кошек коронавирусы вызывают энтериты и инфекционный перитонит, широко распространенные среди диких и домашних кошек.
Возбудителем коронавирусной инфекции у собак является Canine coronavirus, вызывающий острый коронавирусный энтерит. Заболевание передается при непосредственном контакте с носителем вируса (через слюну и фекалии). Данной инфекции подвержены собаки любого возраста, однако чаще всего поражаются щенки и ослабленные животные, которые уже перенесли другую болезнь, например парвовирусную инфекцию.
Основные симптомы заболевания — рвота и диарея, иногда с примесью крови, обезвоживание организма, потеря в весе, апатия. Через 3-4 недели после выздоровления может развиться повторное заболевание. При проведении диагностики коронавирусный энтерит собак необходимо дифференцировать от парвовирусного энтерита, аденовирусной инфекции кишечного типа и чумы плотоядных.
Коронавирусы, поражающие кошек, представлены двумя биотипами: FECV, или коронавирус энтерита кошек, и FIPV — вирус инфекционного перитонита кошек (2, 3). Носителями FECV является 16-50% домашних кошек, у которых вирус локализуется в тонком кишечнике, не вызывая заболевания или становясь причиной легкой диареи. В то же время у 5-12% носителей может наблюдаться мутация условно-патогенной кишечной формы FECV в патогенную (FIPV), что приводит к развитию болезни (2).
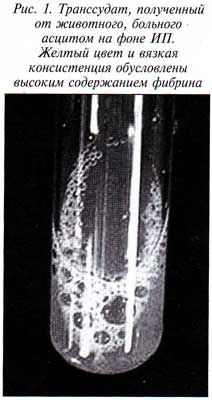
Инфекционный перитонит (ИП, FIP) кошек, заканчивающийся, как правило, летально, протекает в двух формах — влажной и сухой. Влажная (экссудативная) форма ИП характеризуется поражением кровеносных сосудов брюшной или грудной полостей, сопровождающимся выпотеванием плазмы в указанные полости (рис. 1). У больных животных, развивается асцит (рис. 2), а в случае скопления жидкости — нарушение функции дыхания. На серозных покровах органов брюшной полости формируются фибринозные наложения (рис. 3), в дальнейшем могут образовываться спайки. Вследствие нарушения функции печени наблюдается эктеричность склер и кожных покровов.


Сухая (неэкссудативная) форма ИП протекает без скопления жидкости в брюшной и грудной полостях. В этом случае страдают внутренние органы — головной мозг (рис. 4), печень, почки, поджелудочная железа, в 25% случаев наблюдаются поражения глаз (рис. 5) (5).
Поскольку эффективная схема лечения ИП пока не разработана, первостепенное значение имеют профилактические меры, направленные на раннее выявление вирусоносительства (1, 3).
Диагностика инфекционного перитонита кошек также представляет серьезную проблему. Традиционные методы выявления возбудителя, основанные на обнаружении антител к коронавирусам (РНГАи ИФА), дают до 60% ложноположительных результатов. Это обусловлено присутствием в кишечнике кошек условно-патогенных штаммов возбудителя (2, 3). В ряде зарубежных лабораторий применяется комплексная методика диагностики ИП, включающая определение:
— титра антител к коронавирусу;
— соотношения альбуминов/глобулинов в транссудате или плазме крови;
— уровня а-1 кислого гликопро-теина (AGP);
— цитологических и гематологических показателей (4).
Материалы и методы
В исследовании был использован штамм коронавируса «Багира» (5 1оg ТЦД50/мл) в разведениях, 8 изолятов коронавирусов кошек (FCoV), 2 изолята коронавируса собак (CCV) и суспензии вируса панлейкопении кошек и калицивируса кошек.
При испытании ПЦР-тест-системы использовался биологический материал здоровых кошек, животных с клиническими признаками ИП и кошек с неспецифическими симптомами. Среди исследованных животных были как содержащиеся в питомниках, так и находящиеся на индивидуальном содержании.
Биологический материал параллельно исследовался методами ПЦР и РИГА. С помощью ПЦР-системы исследовались фекалии, плазма крови, транссудат при специфическом асците, а методом РИГА — сыворотка крови и транссудат.
Серологические тесты проводились с использованием набора для выявления антител к коронавирусам плотоядных в РИГА (ТУ 9388-025-00494189-01). Биологический материал собак исследовался методом ПЦР.
Однако данное исследование требует значительных затрат времени и средств. В связи с этим эффективным методом диагностики ИП может служить полимеразная цепная реакция (ПЦР), которая позволяет не только выявлять коронавирусы кошек, но и проводить дифференциацию условно-патогенных и патогенных штаммов исходя из различной локализации их в организме. При этом обнаружение вируса в фекалиях кошек свидетельствует о носительстве условно-патогенных штаммов (FECV), а в плазме крови или асцитной жидкости — о циркуляции в организме животного патогенных штаммов (FIPV) и, следовательно, о заболевании.
Цель настоящего исследования — испытание тест-системы для диагностики коронавирусной инфекции у кошек и собак на основе ПЦР.
Выделение РНК проводилось с использованием набора «РНК-сорб» (ЦНИИЭ), в основе которого лежит метод ее сорбции на силикагеле. ПЦР проводилась на амплификаторе ТЕРЦИК («ДНК-технология») по стандартной методике. Полученные ПЦР-продукты визуализировались методом электрофореза в 1,5% агарозном геле, содержащем бромистый этидий.
Результаты и обсуждение
В процессе исследования проведен анализ сведений о нуклеотидных последовательностях представителей семейства Coronaviridae, в частности различных изолятов коронавирусов кошек и собак, опубликованных в базах данных Entrez, GeneBank, EMBL и DDBJ. Кроме того, изучена литература, характеризующая структуру геномов FCoV, CCV и их генетическое родство с другими представителями семейства.
В качестве мишеней для специфических праймеров были выбраны две консервативные последовательности в гене нуклеокапсидного протеина. Специфичность предложенных праймеров изучалась с помощью компьютерных программ FASTA и BLASTA. В результате проведенной работы была выявлена гомология выбранных олигонуклеотидов только с генами нуклеокапсидного протеина FCoV и CCV и не обнаружено их значимой гомологии с нуклеотидными последовательностями иных видов семейства Coronaviridae, а также каких-либо других вирусов, бактерий или эукариот. Таким образом, предложенные праймеры, исходя из теоретических расчетов, должны обладать 100% специфичностью.
На следующем этапе исследования были оптимизированы условия выделения РНК вируса и проведения реакции обратной транскрипции и ПЦР, а также определены специфичность и чувствительность ПЦР-анализа. Размер ПЦР-продукта составил 350 пар нуклеотидов. Метод показал 100% специфичность и высокую чувствительность. Обнаружение коронавируса в фекалиях кошек свидетельствовало о носительстве его условно-патогенных штаммов в кишечнике, обнаружение FECV в транссудате и плазме крови — о развитии заболевания.
При исследовании методом РНГА положительным результатом считалось обнаружение у животного титра антител > 1:128. Однако это могло указывать как на вирусоносительство, так и на манифестированную форму инфекции. Кроме того, положительный титр мог быть обусловлен наличием контакта с коронавирусом ранее. В качестве материала от собак исследовались фекалии, и обнаружение в них РНК коронавируса свидетельствовало о заболевании, вызванном CCV.
В ходе эксперимента был исследован биологический материал, взятый у 193 кошек (таблица). Методом РНГА положительный результат был зафиксирован у 131 животного (титры антител > 1:128). При тестировании «сероположительных» кошек методом ПЦР РНК коронавируса была обнаружена в плазме и асцитной жидкости у 12 животных (9%), только в фекалиях - у 68 (52%) и у 51 (39%) - не обнаружена вовсе. Таким образом, 52% кошек с серопозитивным результатом являлись носителями условно-патогенных штаммов коронавируса, а 39% были здоровы. Очевидно, что исследование методом РНГА дало 63% ложноположительньгх результатов (в пересчете на общее количество исследованных животных).
Заключение
Полученные результаты свидетельствуют о том, что диагностика коронавирусной инфекции кошек традиционным серологическим методом (РНГА) дает более 60% ложноположительных результатов, поскольку не позволяет дифференцировать состояние носительства от истинного заболевания. Кроме того, "сероположительными» считались животные, имевшие контакт с коронавирусом ранее.
Использование метода ПЦР позволило провести дифференциацию условно-патогенных и патогенных штаммов в связи с их раз личной локализацией в организме и отличить состояние носительства от заболевания. Таким образом, данные проведенного исследования говорят о целесообразности использования метода ПЦР для выявления коронавирусов кошек и собак и постановки окончательного диагноза.
В соответствии с приказом № 45 Департамента ветеринарии МСХ РФ в период с 03.08.2004 г. по 06.08.2004 г. были проведены комиссионные испытания тест-системы для диагностики инфекционного перитонита кошек методом ПЦР. Тест-система успешно прошла комиссионную апробацию, показав 100% специфичность и высокую чувствительность в рамках предложенной панели. В настоящее время тест-система «Коронавир» для выявления и идентификации коронавирусов кошек и собак, основанная на ПЦР, успешно используется в ветеринарной практике (ТУ 9388-142-00494189-05; РУ № Р077-1-3.5-0813 зарегистрирована в РФ за № ПВР-1-3.5/01556 от 30.06.06 г. сроком на 5 лет).
ЛИТЕРАТУРА
1, Addie, D, D„ Jarrett, 0. Use of a reverse- transcriptase polymerase chain reaction for monitoring the shedding of feline coronavirus by healthy cats, Vet. Rec, 2001, May 26; 148 (21): 649-53,
2, Vennema, H, atal. Feline Infectious Peritonitis Viruses Arise by Mutation from Endemic Feline Enteric Coronaviruses, Virology, 1998:150-157.
3, Herrewegh, A.A., Mahler, M„ Hedrich, H.J., Haagmans, B.L Egberink, H.F., Horzinek, M.C., Rottier, P.J., de Groot, R,J, Persistence and evolution of feline coronavirus in a closed cat-breeding colony Virology 1997, Aug 4; 234 (2): 349-363,
4, Comparison of Different Tests to Diagnose Feline Infectious Peritonitis; Katrin Hartmann at al„ 2003.
5, Feline infectious peritonitis; Stacy E, Andrew, Veterinary clinics of North America: small animal; vol. 30, number 5, September 2000
Е.А. ЯРАЛОВА, И.Л. ОБУХОВ, ММ РАХМАНИНА, Э.И. ЭЛИЗБАРАШВИЛИ, В.И.УЛАСОВ,
Всероссийский государственный центр качества и стандартизации лекарственных средств для животных и кормов, г. Москва
|


